Der zelluläre Code zum Recyceln
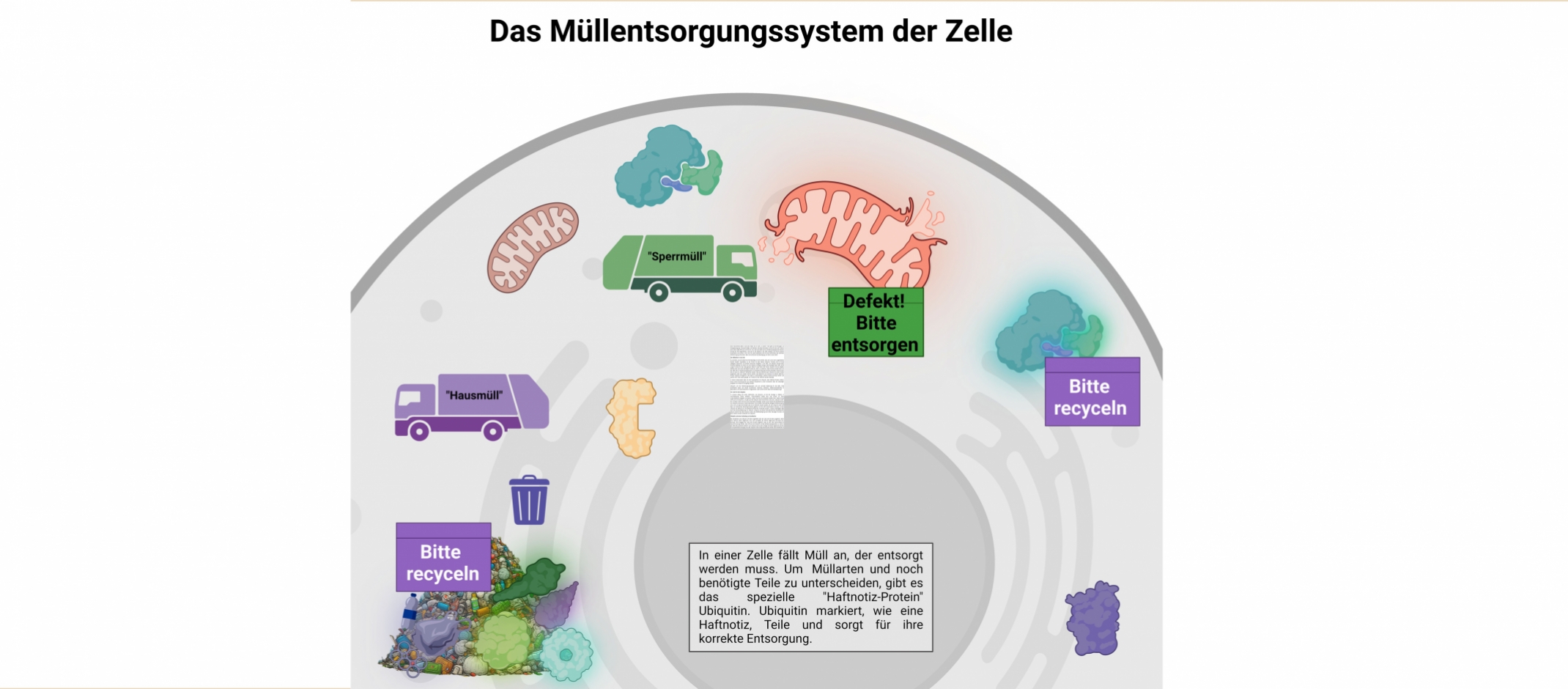
Eine menschliche Zelle ist wie eine Stadt. Sie ist stets „in action“. Dort gibt es Einrichtungen zur Energieerzeugung, Transportstraßen und Fabriken, die etwas herstellen. Es herrscht also viel Trubel in einer Zelle. Dabei fällt auch viel Müll an. Gut, dass eine Zelle auch ein Müllentsorgungssystem besitzt! Würde der Müll liegenbleiben, wäre das für die Abläufe in der Zelle schädlich und könnte letztlich Krankheiten verursachen. Und in der Tat, viele Krankheiten sind mit einer Fehlfunktion der zellulären Müllentsorgung verbunden. Aber wie funktioniert die Beseitigung von Müll in einer Zelle?
Die Müllabfuhr in der Zelle
Zu verstehen, wie eine Zelle ihren Müll beseitigt, ist nicht einfach, da es sich um ein sehr ausgetüfteltes System handelt. Hauptakteur ist ein Protein mit dem Namen Ubiquitin. Proteine sind im Prinzip zelleigene Maschinen und erfüllen bestimmte Aufgaben in der Zelle. Zum Beispiel transportieren Proteine Moleküle von einem Ort zum anderen, erzeugen Energie, oder beseitigen eben Müll. Somit sorgen Proteine für den reibungslosen Ablauf in einer Zelle. Das Protein Ubiquitin hat die Aufgabe, defekte oder nicht mehr benötigte Proteine als „Müll“ zu markieren. Diese Proteine werden dann von der Zelle über ihr Müllentsorgungssystem mit speziellen Recycling-Proteinen beseitigt. Ubiquitin kann also als eine Art „Haftnotiz“ betrachtet werden. Wie eine Haftnotiz kann Ubiquitin an einem Protein angebracht, aber auch wieder entfernt werden. Das Markieren von Proteinen mit diesem Haftnotiz-Protein Ubiquitin ermöglicht es der Zelle zu unterscheiden, welche Proteine entsorgt werden und welche nicht. Oder anders gesagt, nur Proteine mit der Haftnotiz werden beseitigt.

"In meiner Doktorarbeit habe ich mich hauptsächlich mit Ubiquitin, dem Haftnotiz-Protein, befasst. Durch meine Forschung kann ein weiteres Mosaikstück zu dem Verständnis über die vielseitigen Aufgaben von Ubiquitin hinzugefügt werden."
Simon Maria Kienle
Ubiquitin und das Müllentsorgungssystem sind von zentraler Bedeutung für die Zelle. Viele Krankheiten lassen sich darauf zurückführen: Parkinson, Alzheimer, Gebärmutterhalskrebs im Besonderen und viele Krebsarten im Allgemeinen. Aber woher kommt diese zentrale Bedeutung?
Ein Code für viele Aufgaben
In unserem Alltag sind solche Haftnotizen, wie Ubiquitin, um bei der Analogie zu bleiben, in verschiedensten Farben erhältlich. Unterschiedliche Farben kann man nutzen, um ihnen unterschiedliche Aufgaben zuzuweisen, sodass man eine Art Farbcode erstellen kann. Dieses Prinzip trifft auch auf Ubiquitin zu. Es gibt auch bei Ubiquitin einen bestimmten Code, den „Ubiquitin-Code“. Nur ist dieser Code nicht durch ein Farbschema hinterlegt, sondern durch bestimmte Modifikationen von Ubiquitin, die wie ein Code funktionieren. Durch diesen Code weiß die zelleigene Müllentsorgung, ob es sich um Sperrmüll handelt oder ob ein Kleinteil recycelt werden soll. Der Ubiquitin-Code wird dazu von bestimmten Recycling-Proteinen gelesen und der Müll entsprechend entsorgt. So kann Ubiquitin als Haftnotiz für verschiedenste Müllsorten verwendet werden. In dieser Vielseitigkeit liegt auch die zentrale Bedeutung von Ubiquitin. Ubiquitin und dessen farbcode-ähnliche Modifikationen steuern nämlich fast alle Prozesse rund um die Abfallbeseitigung einer Zelle. Deswegen forschen wir auch intensiv an den Funktionen von Ubiquitin.
Ubiquitin und seine Verbindung zu Krankheiten
Bei Krankheiten wird Ubiquitin oft falsch angeheftet oder der Code nicht korrekt ausgeführt. Wenn eine Haftnotiz falsch angebracht wird, wird womöglich der falsche Gegenstand vernichtet bzw. entsorgt. Wird hingegen der Code nicht korrekt ausgeführt, kann es sein, dass Sperrmüllteile im Hausmüll entsorgt werden. Dies trifft auch auf Ubiquitin und das Müllentsorgungssystem zu. Damit in der Zelle alles problemlos abläuft, muss Ubiquitin auch an den richtigen Proteinen angebracht werden; für die passende Entsorgung muss der Ubiquitin-Code richtig entschlüsselt werden. Bei Krankheiten ist oftmals ein Punkt oder sogar beide dieser Punkte fehlgesteuert. Besonders deutlich wird das bei Gebärmutterhalskrebs. Hier wird unter anderem ein Protein irrtümlich vernichtet, welches das Zellwachstum hemmt. Das führt dann zu einer unkontrollierten Zellvermehrung und schließlich zu Krebs. Dahingegen werden bei Alzheimer kaputte Protein nicht richtig entsorgt. Sprich, der Protein-Müll bleibt in Gehirnzellen liegen und führt dazu, dass sie absterben.
"Jedoch wissen wir bei vielen Krankheiten nicht, was im Ablauf der Müllentsorgung, also im Ubiquitin-Code, schiefläuft. Deshalb habe ich mir das Ziel gesetzt, während meiner Doktorarbeit ein weiteres Stück Ubiquitin-Code zu entschlüsseln."
Simon Maria Kienle
Ein weiteres Stück Ubiquitin-Code aufklären
Diesen vielseitigen Farbcode zu entschlüsseln, ist eine wahre Herkulesaufgabe, denn unsere Zellen benutzen enorm viele Ubiquitin-Modifikationen. Sprich, es gibt eine außerordentlich große Anzahl an Farbvarianten der Haftnotiz. Deswegen sind wir den schlecht erforschten Farben der Haftnotiz auf die Spur gegangen. Wir haben dadurch den noch unbekannten Code hinter einer Farbe des Haftnotiz-Proteins und dessen Aufgabe bei der Müllentsorgung entschlüsselt.
Dazu haben wir im Labor über ein paar Tricks Ubiquitin, also die Haftnotiz, mit der entsprechenden Modifikation selbst hergestellt. Nun war die Frage: Was ist die Aufgabe hinter dieser Farbvariante des Ubiquitin-Codes?
Auf der Suche nach unseren Recycling-Proteinen
Es gibt bestimmte Recycling-Proteine, der zelleigenen Müllentsorung, die den Ubiquitin-Code entschlüsseln können und dann den markierten Müll entsorgen. Dabei lesen diese Recycling-Proteine den Ubiquitin-Code und setzten ihn in die entsprechende Entsorgung um. Dazu binden diese decodierenden Recycling-Proteine spezifisch eine Farbe der Haftnotiz. Für unsere Ubiquitin Modifikation waren diese Recycling-Proteine noch nicht bekannt. Und solang dieses Stück des Ubiquitin-Codes nicht entziffert werden kann, kann auch die Aufgabe, die er beschreibt, nicht verstanden werden. Genau deswegen sind wir der Frage nachgegangen, welche Recycling-Proteine unsere Ubiquitin-Modifikation übersetzen können.
"Dazu haben wir den gesuchten Recycling-Proteinen eine Falle gestellt. Diese Proteine müssen nämlich direkt an unser Haftnotiz-Protein Ubiquitin binden, um den Code zu lesen. Das haben wir ausgenutzt. Wenn wir bei der Analogie der Zelle als Stadt bleiben wollen, dann könnte man sagen, dass wir in der ganzen Stadt unsere Haftnotiz verteilt haben und dann beobachtet haben, welche Recycling-Proteine zu der Haftnotiz kommen und gebunden bleiben. Sprich, unsere Ubiquitin war der Köder für die zelluläre Müllabfuhr."
Simon Maria Kienle
Und in der Tat konnten wir dabei Recycling-Proteine finden. Sogar relativ viele Proteine gingen uns in die Falle. Eines jedoch stach besonders heraus: Das war das Protein mit dem Namen „NDP52“. NDP52 ging nämlich sehr häufig in die Falle, was natürlich unsere Aufmerksamkeit weckte. Außerdem ist NDP52 sehr interessant, da es bei der Beseitigung von bakteriellen Krankheitserregern eine wichtige Rolle spielt. Zu diesen Krankheitserregern gehören unter anderem Salmonellen. Wir versuchten also unsere Ergebnisse zu bestätigen – mit Erfolg! NDP52 zeigte in allen weiteren Versuchen eine starke Bindung zu unserer Ubiquitin-Haftnotiz. Das heißt, NDP52 ist eines der Recycling-Proteine für unseren Teil des Ubiquitin-Codes. So nehmen wir an, dass unser Stück Ubiquitin-Code dazu beiträgt, große Sperrmüllteile, wie zum Beispiel ganze Bakterien, zu beseitigen. Im Allgemeinen lässt sich durch unsere Forschung mit NDP52 und den anderen gefundenen Recycling-Proteinen die Aufgabe unseres Stücks Ubiquitin-Code besser verstehen. In Zukunft kann dieses Wissen sogar zur Entwicklung neuer Medikamente gegen Krankheiten ausgenutzt werden.
Simon Maria Kienle promovierte am Fachbereich Biologie zum Thema posttranslationale Modifikation von Proteinen und deren Wirkungsweisen. Er schloss seine Promotion im Jahr 2022 ab und forscht heute als Postdoc an der Realisierung von personalisierter Medizin am Steno Diabetes Center in Kopenhagen, Dänemark. Hier begibt er sich mittels „-omics“ Technologien auf die Spurensuche nach Molekülen, die es erlauben, einen Krankheitsverlauf zuverlässig vorherzusagen. Die ursprüngliche Fassung dieses Artikels reichte er zum KlarText-Wettbewerb 2023 der Klaus Tschira Stiftung ein.